Artikelen
Artikelen - Wondkweken bij chronische ulcera, de do’s en don’ts (2019-03)
Het ulcus cruris gaat vaak gepaard met een gecompliceerd en belastend ziektebeloop waarbij de kwaliteit van leven aanzienlijk daalt. [1] De prevalentie ligt op 1% bij de volwassen populatie en 3-5% bij mensen boven de 65 jaar. [2] De onderliggende oorzaken van ulcera crures zijn legio (figuur 1). [3] We zullen ons toespitsen op het ulcus cruris venosum en diabeticum.
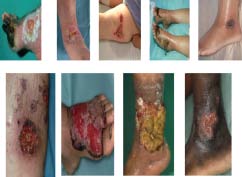
Figuur 1. Chronische ulcera crures.
De prevalentie van infectie bij patiënten met een ulcus cruris was in een onderzoek in Australië bij 561 patiënten op het moment van inclusie 7,8%. [4] Na afname van een wondkweek wordt dan logischerwijze aangevangen met systemische antibiotica. Het afnemen van een wondkweek bij een patiënt met een ulcus cruris zonder klinische tekenen van infectie en het routinematig behandelen met antibiotica komt echter ook nog vaak voor. Maar is dit wetenschappelijk verantwoord? Hieronder wordt een overzicht gegeven van de landelijke en internationale richtlijnen.
Wondkweken bij het ulcus cruris venosum
Volgens de internationale en landelijke richtlijnen van het ulcus cruris venosum is het niet zinvol om routinematig wondkweken af te nemen of systemische antibiotica te starten bij ulcera zonder klinische aanwijzingen voor infectie. Dit zou bij kunnen dragen tot resistentie (tabel 1, figuur 2).
Klinische aanwijzingen voor infectie zijn rubor, calor, dolor, tumor, functio laesa en koorts.
Alle wonden verliezen enkele uren na ontstaan hun steriliteit. Er wordt onderscheid gemaakt tussen gecontamineerde (niet- delende bacteriën van de eigen huidflora en omgeving), geko- loniseerde (delende bacteriën veelal huidbacteriën, die geen schade veroorzaken) en geïnfecteerde wonden (delende bacte- riën die schade veroorzaken). De progressie van contaminatie naar infectie hangt af van het aantal bacteriën, de virulentie en de afweer van de gastheer. Bij het afnemen van een wond- kweek zonder klinische tekenen van infectie zal deze in vele gevallen ook positief zijn (in 95% van de gevallen bij veneuze ulcera en in 70% van de gevallen bij diabetische ulcera). [5] Zoals de internationale richtlijn voor veneuze ulcera aangeeft is een wondkweek niet de indicatie tot behandeling, maar dient als leidraad voor het kiezen van therapie. [6] Daarnaast is er geen wetenschappelijk bewijs dat er een relatie bestaat tussen de microbiële belasting of bepaalde moleculaire kenmer- ken van bacteriën in het ulcus cruris venosum en vertraagde genezing. [6] Een gerandomiseerde studie heeft bovendien aangetoond dat er geen verschil is in de wondgenezing tussen patiënten met niet-geïnfecteerde chronische veneuze ulcera die antibiotica kregen naast compressietherapie en patiënten die geen antibiotica hiernaast kregen voorgeschreven. [7]
Er is samengevat geen plaats voor het routinematig voorschrijven van antibiotica bij het ulcus cruris venosum.
De meeste kweken laten een groei zien van S. aureus, P. aerugi- nosa, P. mirabilis en hemolytische streptokokken. Hiermee moet rekening worden gehouden bij het blind voorschrijven van antibiotica (tabel 1). [8] Valkuilen bij gebruik van antibio- tica zijn het starten van therapie bij een niet-geïnfecteerde maar een gekoloniseerde wond, de verwekker van de infectie wordt niet aangetoond, microbiologische resultaten worden genegeerd of patiënten nemen de antibiotica niet in. Er wordt aanbevolen om voor het maken van een antibioticumkeuze eerst de ziekenhuisrichtlijn te raadplegen. Een consult microbiologie wordt geadviseerd.
Het gebruik van lokale antibiotica wordt niet aanbevolen vanwege de ontwikkeling van resistentie en contactallergie (sofra-, genta- en neomycine maar ook voor andere producten zijn allergische reacties beschreven). Azijnzuur wordt in de praktijk vaak toegepast bij ulcera met een pseudomonasinfec- tie zonder wetenschappelijk bewijs, maar volgens experts wel naar tevredenheid. De werkzaamheid van honing- en zilverbe- vattende wondbehandelingsproducten (in crèmes/dressings) bij patiënten met een ulcus cruris venosum is niet aangetoond. Voor de overige middelen met antibacteriële werking zoals fusidinezuur, ethacridinelactaat, mupirocine en chloorhexi- dine bij de behandeling van ulcus cruris is tot op heden geen meerwaarde beschreven. Cadexomeerjodium is het enige werkzame product wanneer toepassing van een middel met antibacteriële werking wordt overwogen (tabel 1). [6,9]
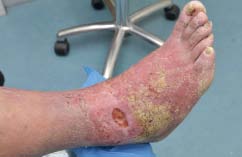
Figuur 2. Ulcus cruris venosum.
Tabel 1. Beleid wondkweken en antibiotica bij het ulcus cruris venosum.
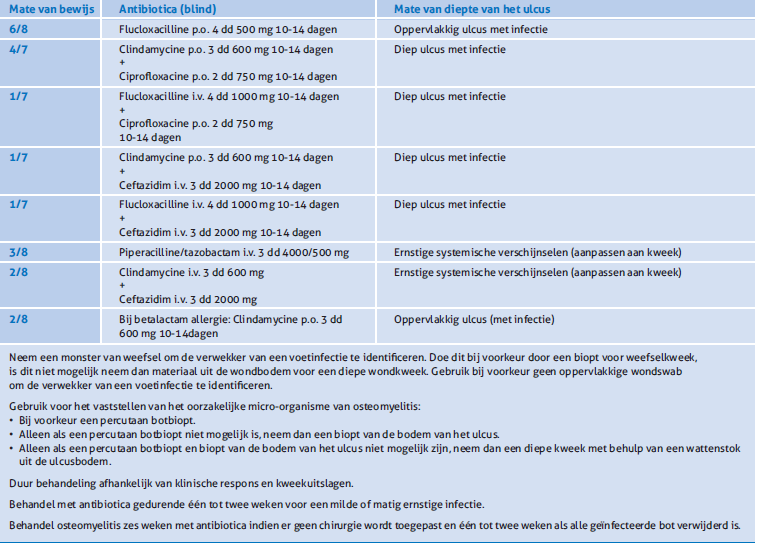
Tabel 2. Antibioticabeleid bij het diabetisch ulcus (SWAB). [12]
Wondkweken bij het ulcus diabeticum
Wat betreft het ulcus diabeticum bevelen zowel de landelijke als internationale richtlijnen aan om alleen bij klinische ver- denking op infectie een ‘diepe’ wondkweek af te nemen door curettement van de wondbodem na een initieel debridement (verwijderen van oppervlakkig beslag). Niet alle kenmerken van infectie hoeven aanwezig te zijn door neuropathie en vaatlijden. [10] Ongeveer de helft van alle diabetische ulcera raakt geïnfecteerd. [11]
Een oppervlakkige wonduitstrijk is niet geschikt om de ver- wekker van een geïnfecteerd diabetisch ulcus te identificeren. Het herhaaldelijk afnemen van kweken wordt afgeraden tenzij de behandeling met antibiotica niet het gewenste effect geeft. Beoordeel de uitgebreidheid van de infectie op basis van klinische symptomen, aanvullend laboratoriumonderzoek, aanwezigheid van wondondermijning en diepte van de wond. Bij een niet-oppervlakkige wond dient een röntgenfoto gemaakt te worden om osteomyelitis uit te sluiten. De landelijke richt- lijn voor de keuze van antibiotica vermeldt flucloxacilline voor een oppervlakkig ulcus en voor een diep ulcus clindamycine met flucloxacilline, clindamycine met ciprofloxacine, clinda- mycine met ceftazidim of flucloxacilline met ceftazidim.
Bij een uitgebreide infectie wordt gekozen voor piperacillin- tazobactam of ceftazidim met clindamycine. De duur van de behandeling varieert van tien tot veertien dagen (tabel 2). [12,13] De internationale richtlijn wijkt niet af van de nationale richtlijn. [10,11] Ook hier is het belangrijk om de ziekenhuisrichtlijn eerst te raadplegen.
Bij een geïnfecteerd diabetisch ulcus is het noodzakelijk om de wond te sonderen, in het geval het bot palpabel is, is de diagnose osteomyelitis uiterst waarschijnlijk. In dit geval volstaat zes weken antibiotica. Indien het geïnfecteerde bot verwijderd wordt is een week orale antibiotica voldoende.
Uiteraard is een positieve botkweek het ultieme diagnosticum, dit is echter niet altijd mogelijk. Vermeldingswaardig is dat meer dan 50% van de patiënten met een diabetisch ulcus binnen vijf jaar overlijdt (mortaliteit vergelijkbaar met coloncarcinoom) en ongeveer 5% een ledemaat verliest. [14] Antibiotische therapie bij de diabetische voet is moeizaam aangezien er vaak sprake is van arteriële insufficiëntie, resis- tentie van pathogene bacteriën (met name de S. aureus en Pseudomonas) en verminderde nierfunctie wat de keuze voor antibiotica bemoeilijkt.
Er is onvoldoende bewijs voor de werkzaamheid van antisepti- sche of antimicrobiële middelen (honing-, zilver- of jodiumbe- vattende producten) in de behandeling van het geïnfecteerde diabetisch ulcus. Het advies is de wondbedekker te gebruiken die de minste druk geeft in de schoen en die wondgenezing in een vochtmilieu mogelijk maakt tegen de laagste prijs. [15]
Biofilms
Afgelopen jaren is er steeds meer bekend geworden over bacteriën die niet in planktonvorm (vrij) leven, maar verankerd zijn aan het wondoppervlak en met elkaar communiceren. De eerste kolonisten maken polysachariden aan om zich te hech- ten aan het wondoppervlak. Deze polysachariden vormen een goede basis voor het hechten van nog meer micro-organismen die op hun beurt weer polysachariden vormen. Het geheel wordt ook wel een biofilm genoemd. [16-18] Biofilms beschermen de micro-organismen tegen de buitenwereld door het creëren van een gunstige micro-omgeving, verhoogde virulentie en het afbreken van voedingsstoffen resulterend in resistentie tegen het immuunsysteem en antibiotica. [14] Ze komen in 60% voor bij chronische wonden versus 6% bij acute wonden. Stafylokokken, P. aeruginosa en enterokokken komen het meeste voor in biofilms. [18] Onderzoek heeft aangetoond dat plasma- en glucosebevattende media leiden tot de ontwikke- ling van de dikste biofilms. Hetzelfde onderzoek heeft aange- toond dat het diabetisch ulcus van alle wonden de meeste biofilmlading bevat. [18,19] De behandeling van biofilms be- staat voor een groot deel uit wonddebridement en een lokaal antibiofilmsepticum. [20] Hoewel er nog geen consensus is over antibiofilmseptica, zijn lactoferine en xylitol in combinatie met hydrogel en zilvernitraatwondbedekkers, 5% theeboom- olie (tea trea oil), bismutthiolen en biocellulose wondbedek kers met polyhexanide mogelijk effectief gebleken. [18,21-24] Het gebruik van D-aminozuren zou de effectiviteit van antibiotica mogelijk vergroten. [25]
Voorlopig is mechanisch debrideren de hoeksteen van de behandeling van biofilms.
Literatuur
- Heyer K, Herberger K, Protz K, Glaeske G, Augustin M. Epidemiology of chronic wounds in Germany: Analysis of statutory health insurance data. Wound Repair Regen 2016;24(2):434-42.
- Mekkes JR, Loots MA, van der Wal AC, Bos JD. Causes, investigation and treatment of leg ulceration. Br J Dermatol. 2003;148(3):388-401.
- Jockenhofer F, Gollnick H, Herberger K, et al. Aetiology, comorbidities and cofactors of chronic leg ulcers: retrospective evaluation of 1000 patients from 10 specialised dermatological wound care centers in Germany. Int Wound J 2016;13(5):821-8.
- Bui UT, Edwards H, Finlayson K. Identifying risk factors associated with infection in patients with chronic leg ulcers. Int Wound J 2018;15(2):283-90.
- Schmidt K, Debus ES, St J, Ziegler U, Thiede A. Bacterial population of chronic crural ulcers: is there a difference between the diabetic, the venous, and the arterial ulcer? Vasa 2000;29(1):62-70.
- Couch KS, Corbett L, Gould L, Griolami S, Bolton L. The international consolidated venous ulcer guideline update 2015: process improve- ment, evidence analysis, and future goals. Ostomy Wound Manage 2017;63(5):42-6.
- Alinovi A, Bassissi P, Pini M. Systemic administration of antibiotics in the management of venous ulcers. A randomized clinical trial. J Am Acad Dermatol 1986;15(2 Pt 1):186-91.
- Madsen SM, Westh H, Danielsen L, Rosdahl VT. Bacterial colonization and healing of venous leg ulcers. APMIS 1996;104(12):895-9.
- Richtlijn Veneuze pathologie. Nederlandse Vereniging voor Dermato- logie en Venereologie (NVDV), 2014.
- Lipsky BA, Aragon-Sanchez J, Diggle M, et al. IWGDF guidance on the diagnosis and management of foot infections in persons with diabetes. §Diabetes Metab Res Rev 2016;32 Suppl 1:45-74.
- Peters EJ, Lipsky BA. Aragon-Sanche J, et al. Interventions in the management of infection in the foot in diabetes: a systematic review. Diabetes Metab Res Rev 2016;32 Suppl 1:145-53.
- https://swabid.nl/node/6714. Stichting werkgroep antibioticabeleid SWABID (nationaal).
- https://richtlijnendatabase.nl/richtlijn/diabetische_voet/behande ling/behandeling_diabetische_voetinfectie.html. NIV Richtlijn Diabetische Voet 2017.
- Kalan LR, Brennan MB. The role of the microbiome in nonhealing diabetic wounds. Ann NY Acad Sci 2019;1435(1):79-92.
- Game FL, Attinger C, Hartemann A, et al. IWGDF guidance on use of interventions to enhance the healing of chronic ulcers of the foot in diabetes. Diabetes Metab Res Rev 2016;32 Suppl 1:75-83.
- Gompelman M, van Asten SA, Peters EJ. Update on the role of infec- tion and biofilms in wound healing: Pathophysiology and treatment. Plast Reconstr Surg 2016;138(3 Suppl):61S-70S.
- Wu YK. Cheng NC, Cheng CM. Biofilms in chronic wounds: pathogene- sis and diagnosis. Trends Biotechnol 2018 Nov 26. pii: S0167- 7799(18)30307-X.
- Kravvas G, Veitch D, Al-Niaimi F. The increasing relevance of biofilms in common dermatological conditions. J Dermatolog Treat 2018;29(2):202-7.
- Kwiecinski J, Kahlmeter G, Jin T. Biofilm formation by Staphylococcus aureus isolates from skin and soft tissue infections. Curr Microbiol 2015;70:698-703.
- Schultz G, Bjarnsholt T, James GA, et al. Consensus guidelines for the identification and treatment of biofilms in chronic nonhealing wounds. Wound repair regen 2017;25(5):744-57.
- Ammons MC, Ward LS, Garth JA. Anti-biofilm efficacy of a lactofer- rin/xylitol would hydrogel used in combination with silver nitrate wound dressings. Int Wound J 2011;8:268-73.
- Brady A, Loughlin R, Gilpin D, et al. In vitro activity of teatree oil against clinical skin isolates of meticillin-resistant and -sensitive Staphylococcus aureus and coagulase-negative staphylococci growing planktonically and as biofilms. J Med Microbiol 2006;55:1375-80.
- Folsom JP, Baker B, Stewart PS. In vitro efficacy of bismuth thiols against biofilms formed by bacteria isolated from human chronic wounds. J Appl Microbiol 2011;111:989-96.
- Lenselink E, Andriessen A. A cohort study on the efficacy of a poly- hexanide-containing biocellulose dressing in the treatment of biofilms in wounds. J Wound Care 2011;20:536-9.
Samenvatting
Het ziektebeloop van een ulcus cruris is vaak gecompli- ceerd en belastend voor de patiënt. Ondanks adequate behandeling kan de genezingstendens stagneren. Wond- infectie speelt bij deze patiëntengroep ook vaak parten wat leidt tot meer pijn en sociaal ongemak vanwege riekende ulcera. In dit artikel bespreken we de richtlijnen van het ulcus cruris venosum en het ulcus diabeticum ten aanzien van het afnemen van wondkweken en de behandeling van wondinfectie. Volgens zowel de landelijke als internatio- nale richtlijnen van het ulcus cruris venosum en het diabe- tisch ulcus is het afnemen van wondkweken en starten van systemische antibiotica alleen zinvol als er klinisch een verdenking is op wondinfectie. In alle andere gevallen kan het starten van systemische antibiotica bijdragen aan anti- bioticumresistentie en moet daarom worden afgeraden.
Bij het diabetisch ulcus kan een wondinfectie leiden tot osteomyelitis en niet zelden tot amputatie van een teen of deel van de voet. Alertheid op wondinfectie bij elk consult is vereist.
Ten slotte worden biofilms kort besproken. Uit recent onderzoek blijkt dat biofilms een rol spelen bij het falen van behandeling van wondinfecties. Een biofilm bestaat uit bacteriën omgeven door een polysacharide extracellulaire matrix resistent tegen antibiotica. Toekomstig innovatief onderzoek moet uitwijzen wat de beste strategie is voor het verwijderen van de biofilms. De huidige behandeling betreft voornamelijk herhaaldelijk mechanisch debrideren van de wond.
Trefwoorden
wondkweken – antibiotica – ulcus cruris venosum – ulcus diabeticum
Correspondentieadres
Miriam Loots
E-mail: M.Loots@Fransciscus.nl