Artikelen
Urticaria en geneesmiddelen allergie - Behandeling van patiënten met chronische urticaria met omalizumab* (2019-04)
Artikel in PDF
L.S. Spekhorst, J.M.P.A. van den Reek, A. C. Knulst, H. Röckmann
In verschillende studies, waaronder gerandomiseerd gecontroleerd onderzoek is de effectiviteit en veiligheid van omalizumab in de behandeling van chronische urticaria (CU) aangetoond. [1] Echter, data over de behandeling met omalizumab in de dagelijkse praktijk en in het bijzonder gegevens op de lange termijn ontbreken.
De drug-survivalanalyse is een methode die een weerspiegeling geeft van de dagelijkse praktijk door de verwachte tijdsduur tot een gebeurtenis plaatsvindt te analyseren, in dit geval het staken van de behandeling met omalizumab. Tevens is het een analyse waarbij effectiviteit, veiligheid en voorkeuren van patiënten en artsen wordt meegenomen. [2] We evalueerden de drug survival van omalizumab in een groot cohort van patiënten met CU behandeld in de dagelijkse praktijk. Tevens werden determinanten geïdentificeerd voor de drug survival in de totale populatie en gedifferentieerd voor reden van stoppen.
Methode
Gegevens werden geëxtraheerd uit de medische dossiers van alle patiënten met de diagnose CU, die behandeld zijn met omalizumab in het UMC Utrecht in de periode van februari 2012 tot februari 2018. Het behandelingsprotocol is gebaseerd op de internationale en Nederlandse richtlijnen voor CU. [3,4] Elke patiënt kreeg initieel 300 mg omalizumab elke vier weken toegediend. In het geval van een goed gecontroleerde ziekte (UCT > 12), voor minstens drie maanden, werd het toedieningsinterval van omalizumab per gift verlengd met één week. De behandeling werd gestopt indien CU goed onder controle bleef met een toedieningsinterval van acht weken. Omalizumab werd herstart indien de patiënt een terugval had na stopzetting. Als patiënten onvoldoende reageerden op omalizumab (ten minste vijf opeenvolgende toedieningen met een UCT < 11), werd de dosering verhoogd tot 450-600 mg. Wanneer de respons onvoldoende bleef, werd het interval verkort van vier naar twee weken. Patiënten die niet voldoende reageerden op het verhogen van de dosis en het verkorten van het interval werden beschouwd als non-responders en de behandeling met omalizumab werd gestaakt. Drug survival werd bepaald door middel van kaplanmeieroverlevingscurves en afzonderlijk geanalyseerd voor (I) overall drug survival (stopzetting om welke reden dan ook) en op basis van verschillende redenen voor stopzetting; (II) goed gecontroleerde ziekteactiviteit, (III) bijwerkingen [met/zonder ineffectiviteit], (IV) ineffectiviteit [met/zonder bijwerkingen]. Patiënten die omalizumab gebruikten ten tijde van data lock of niet verder vervolgd werden, werden gecensureerd. Patiënten die omalizumab stopten om andere redenen (bijvoorbeeld zwangerschapswens), werden geclassificeerd als een gebeurtenis in de overall drug survival maar werden gecensureerd in de subanalyses (II, III en IV). Het censureren van data zorgt ervoor dat data van patiënten met verschillende follow-upperioden volledig in het model kunnen worden opgenomen. [2] Van elke patiënt werden gegevens verzameld betreffende patiëntkarakteristieken, behandelingsduur, effectiviteit en reden van stoppen. De volgende variabelen werden geselecteerd als mogelijke determinanten voor de omalizumab drug survival: geslacht, leeftijd, ziekteduur, voorgaande therapieën, auto-immuunziekte, presentatie van spontane en/of induceerbare urticaria, aanwezigheid van angio-oedeem en/of kwaddels, vroege en late response. Potentiële drug-survivaldeterminanten werd geanalyseerd middels een univariaat Cox-regressiemodel waarbij determinanten die verschilden tussen de twee groepen met een p-waarde < 0,2 werden meegenomen in een multivariaat Cox-regressiemodel. Het onderzoek werd voorgelegd aan de Medisch Ethische Commissie, die verklaarde geen bezwaar te hebben tegen deze studie (WAG/mb/17/034482).
* De resultaten van deze studie zijn recent in Allergy gepubliceerd. [5] Dit artikel is een samenvatting van de meest belangrijke data voor Nederlandse collega’s.
Resultaten
Van de 148 gescreende patiënten werden 142 patiënten geïncludeerd met een gemiddelde leeftijd van 42 jaar (SD 14,8), 71% was vrouw. In de totale populatie presenteerde 91% van de patiënten zich met spontane kwaddels (CSU), tevens had 31% van de patiënten ook induceerbare urticaria als hoofd of bijkomende diagnose. Bovendien had 66% van de patiënten klachten van angio-oedeem (CSU) (figuur 1). Patiënten met de hoofddiagnose CSU en bijkomend CindU hadden een significant langere ziekteduur (mediaan 3,0 jaar) vóór aanvang van omalizumabbehandeling in vergelijking met patiënten met CSU zonder CindU (mediaan 2,0 jaar, p = 0,027). Er werden geen significante verschillen gevonden tussen patiënten met een diagnose van CSU of CindU in effectiviteit van omalizumab.
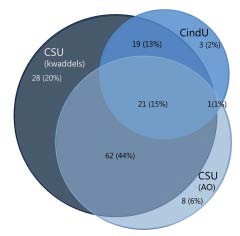
Figuur 1. Verdeling van CU-subtypes.
Legenda: Verdeling CU-subtypes, aanwezigheid van kwaddels (CSU), angio oedeem (CSU) en CindU-type als hoofddiagnose of bijkomende diagnose.
Op het moment van de data lock gebruikten 90 patiënten (63%) omalizumab, 45 patiënten (32%) hadden de behandeling met omalizumab gestaakt en 7 patiënten (5%) waren niet verder vervolgd. De meest voorkomende reden voor stoppen van omalizumab was goed gecontroleerde ziekte; 22 van de 142 patiënten (16%) stopten vanwege deze reden. 7 patiënten (4,9%) staakten de behandeling vanwege ineffectiviteit, 5 patiënten (3,5%) vanwege bijwerkingen en 3 patiënten (2,1%) vanwege een combinatie van zowel bijwerkingen als ineffectiviteit.
De drug-survivalpercentages voor omalizumab waren 77%, 61% en 55% na respectievelijk één, twee en drie jaar en werden voornamelijk bepaald door goed gecontroleerde ziekte (figuur 2). Drug survival gerelateerd aan bijwerkingen en ineffectiviteit was constant na twee jaar, dit betekent dat na twee jaar omalizumabbehandeling geen van de patiënten de behandeling stopte vanwege ineffectiviteit of bijwerkingen. De relatief lange drug survival van omalizumab bij ineffectiviteit/bijwerkingen, ofwel de lange tijdsduur tot het moment van staken kan worden verklaard door partial-responders en afwezigheid van andere effectieve behandelingsopties. Ook leidt intervalverlenging en recidivering van de ziekte met daaropvolgende herstart van de behandeling tot langere drug survival. [7] Na selectie van voorspellers in een univariaat Cox-regressiemodel, identificeerde multivariate Cox-regressieanalyse de aanwezigheid van CindU (als hoofd- of bijkomende diagnose) als een onafhankelijke determinant van langere overall drug survival en langere drug survival (verlaagde kans op stoppen) wegens goed gecontroleerde ziekteactiviteit (figuur 3). Slechts een klein aantal patiënten (n = 15, 11%) staakte de behandeling vanwege bijwerkingen en/of ineffectiviteit waardoor voor deze redenen van stoppen geen multivariate Cox-regressieanalyses werden verricht.
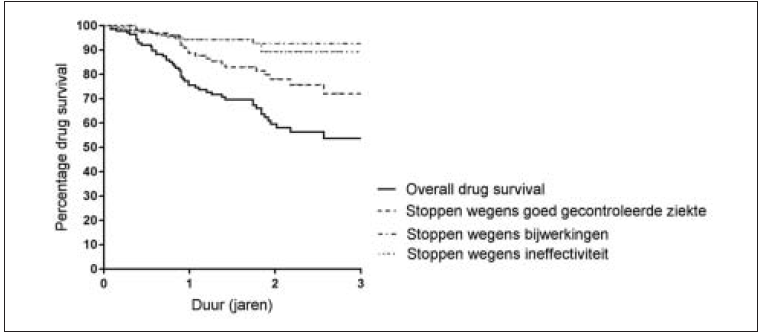
Figuur 2. Omalizumab drug survival in CU.
Legenda: Omalizumab drug survival middels kaplan-overlevingscurves; overall drug surival en de drug survival gedifferentieerd voor reden van stoppen. Een verticale streep in de drug-survivalcurve geeft een patiënt weer op het moment van censureren. De mediane drug survival kon niet worden vastgesteld, aangezien > 50% van de patiënten aan het einde van de studie nog werd behandeld met omalizumab.
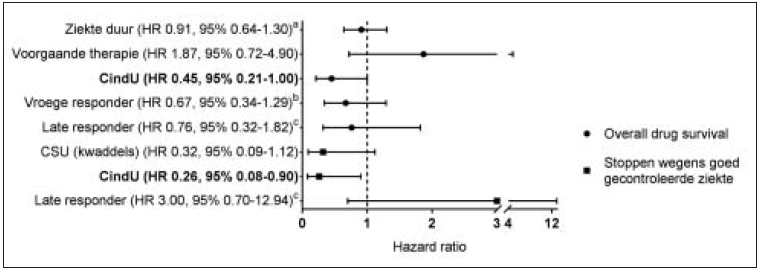
Figuur 3. Determinanten geassocieerd met omalizumab drug survival in CU.
Legenda: Multivariate Cox-regressie voor overall drug survival (stip) en gedifferentieerd voor stoppen vanwege goed gecontroleerde ziekte (vierkant). Data worden gepresenteerd als hazardratio (95% betrouwbaarheidsinterval). Vetgedrukte cijfers geven hazardratio’s aan met een p < 0,05. Vroege responder; T2, UCT-score > 12 binnen 4 weken na de eerste toediening. Late responder; T4, UCT-score > 12 na T2 maar op het tijdstip van de vierde dosis. aziekteduur voor start omalizumab in vijfjaarsinterval; bvroege responder vergeleken met cohort; cvroege en late responder vergeleken met cohort. (UCT = Urticaria Control Test)
Discussie
In deze studie betreffende de dagelijkse praktijk waren de overall drug-survivalpercentages voor omalizumab respectievelijk 77%, 61% en 55% na één, twee en drie jaar. Tot op heden is slechts één drug-survivalanalyse (n = 298) voor omalizumab bij patiënten met CU verricht in de VS. Hierbij gebruikte ten minste 70% van de patiënten na één behandelingsjaar nog omalizumab, met vergelijkbare cijfers als in ons onderzoek. De redenen voor stoppen en determinanten geassocieerd met drug survival werden niet onderzocht. [6] Een Deense dagelijkse praktijk cohortstudie (n = 154) toonde aan dat 56% van de CSU-patiënten na één jaar nog steeds werd behandeld met omalizumab. Voornaamste redenen voor stoppen waren goed gecontroleerde ziekte (16%) en ineffectiviteit (13%). [7] In onze studie werd voor de eerste keer een onderscheid gemaakt tussen CU-types en de associatie met de drug survival van omalizumab. CindU, als hoofd- en bijkomende diagnose, werd geïdentificeerd als determinant voor een langere overall drug survival en langere drug survival gerelateerd aan goed gecontroleerde ziekte. Dit suggereert dat patiënten met CindU minder snel met omalizumab stoppen vanwege een goed gecontroleerde ziekte. CindU was echter niet geassocieerd met een lagere effectiviteit van omalizumab. Voorgaande studies hebben aangetoond dat de aanwezigheid van de bijkomende diagnose CindU bij patiënten met de hoofddiagnose CSU geassocieerd was met langere ziekteduur en een lagere kans op spontane remissie in vergelijking met patiënten met alleen CSU zonder aanwezigheid van CindU. [8-10] In onze studie was de ziekteduur voor de start van de behandeling ook significant langer bij patiënten met de hoofddiagnose CSU en bijkomende diagnose CindU vergeleken met het solitair voorkomen van CSU. Het is mogelijk dat patiënten met de aanwezigheid van CindU een lagere kans hebben op spontane remissie waardoor een langere behoefte aan behandeling met omalizumab bestaat. Dit kan de langere drug survival gerelateerd aan goed gecontroleerde ziekteactiviteit verklaren. De behandelingsrespons tussen CU-subtypen verschilde echter niet significant. Wellicht zijn patiënten met CindU minder snel geneigd om de behandeling te staken vanwege langere ziekteduur of recidiveren ze sneller na een poging tot stoppen. Ook kunnen verschillen in het pathomechanisme tussen CU-subtypen een rol spelen, aangezien de pathofysiologie van CU nog niet volledig wordt begrepen. Een limitatie van deze studie is dat de drug survival wordt beïnvloed door het gedrag van artsen en/of patiënten met betrekking tot het voorschrijven en stoppen van omalizumab [11], dit wordt gedeeltelijk tenietgedaan door protocollen. De generalisatie van onze resultaten kan beperkt zijn door verschillen in lokale/nationale behandelingsprotocollen tussen ziekenhuizen/landen. Verdere multicenterstudies zijn nodig uit verschillende ziekenhuizen/landen om inzicht te krijgen in deze mogelijke verschillen.
Conclusie
In deze studie over de dagelijkse praktijk met een observatieperiode tot zes jaar, waren de overall drug-survivalpercentages voor omalizumab 77%, 61% en 55% na respectievelijk één, twee en drie jaar. Dit betekent dat de meerderheid van de patiënten gedurende meerdere jaren wordt behandeld met omalizumab. De voornaamste reden voor het stoppen van omalizumab was goed gecontroleerde ziekte, 49% van de gestopte patiënten stopte vanwege deze reden. De aanwezigheid van CindU, zowel als hoofd- en als bijkomende diagnose, leidde tot een langer gebruik van omalizumab.
Literatuur
1. Kaplan A, Ledford D, Ashby N, et al. Omalizumab in patients with symptomatic chronic idiopathic/spontaneous urticaria despite standard combination therapy. J Allergy Clin Immunol 2013;132(1):101-9.
2. van den Reek JMPA, Kievit J, Gniadecki R, et al. Drug survival studies in dermatology: Principles, purposes, and pitfalls. J Invest Dermatol 2015;135(7):1-5.
3. Zuberbier T, Aberer W, Asero R, et al. The EAACI/GA(2)LEN/EDF/WAO guideline for the definition, classification, diagnosis and management of urticaria. Allergy 2018;73(7):1393-414.
4. Nederlandse Vereniging voor Dermatologie en Venereologie. Multidisciplinaire evidence based richtlijn Chronische spontane urticaria, 2015.
5. Spekhorst LS, van den Reek JMPA, Knulst AC, Röckmann H. Determinants of omalizumab drug survival in a long-term daily practice cohort of patients with chronic urticaria. Allergy 2018 Dec 28.
6. Ke X, Kavati A, Wertz D, et al. Real-world characteristics and treatment patterns in patients with urticaria initiating omalizumab inthe United States. J Manag Care Spec Pharm 2017 dec 19:1-11.
7. Ghazanfar MN, Sand C, Thomsen SF. Effectiveness and safety of omalizumab in chronic spontaneous or inducible urticaria: evaluation of 154 patients. Br J Dermatol 2016;175(2):404-6.
8. Sanchez-Borges M, Caballero-Fonseca F, Capriles-Hulett A, et al. Factors linked to disease severity and time to remission in patients with chronic spontaneous urticaria. J Eur Acad Dermatol Venereol 2017;31(6):964-71.
9. Kozel MM, Mekkes JR, Bossuyt PM, Bos JD. Natural course of physical and chronic urticaria and angioedema in 220 patients. J Am Acad Dermatol 2001;45(3):387-91.
10. Curto-Barredo L, Archilla LR, Vives GR, Pujol RM, Giménez-Arnau AM. Clinical Features of chronic spontaneous urticaria that predict disease prognosis and refractoriness to standard treatment. Acta Derm Vene- reol 2018;98(7):641-7.
11. Kolkhir P, Pogorelov D, Darlenski R, et al. Management of chronic spontaneous urticaria: a worldwide perspective. World Allergy Organ J 2018;11(1):14.
Samenvatting
Verscheidene studies hebben aangetoond dat omalizumab effectief is voor het behandelen van chronische urticaria (CU). Echter, langetermijndata, specifiek drug-survival- studies, voor effectiviteit en veiligheid van omalizumab bij patiënten met CU in de dagelijkse praktijk ontbreken. Het doel van deze studie was het evalueren van de drug survival van omalizumab in een groot CU-cohort in de dagelijkse praktijk. Tevens werd getracht determinanten te identificeren voor de overall drug survival en drug survival per reden van stoppen. Data werden geëxtraheerd uit een prospectief cohort (februari 2012 tot februari 2018) van CU-patiënten die behandeld werden met omalizumab in het UMC Utrecht. Drug survival werd geanalyseerd met behulp van de Kaplan-overlevingscurve. Determinanten voor drug survival werden geïdentificeerd door univariate en multivariate Cox-regressieanalyse. In totaal werden 142 patiënten (71% vrouw, gemiddelde leeftijd 42 jaar) met een maximale behandelingsduur van 4,7 jaar (209 actieve behandelingsjaren) geïncludeerd. De drug-survivalpercentages voor omalizumab waren 77%, 61% en 55% na respectievelijk 1, 2 en 3 jaar, en werden voornamelijk bepaald door goed gecontroleerde ziekte. Weinig patiënten stopten de behandeling vanwege ineffectiviteit en/of bijwerkingen. Chronische induceerbare urticaria (CindU), zowel als hoofd- en als bijkomende diagnose, was geassocieerd met langere overall drug survival en langere drug survival gerelateerd aan goed gecontroleerde ziekte.
Trefwoorden
drug survival – chronische urticaria – dagelijkse praktijk – determinanten – omalizumab
Correspondentieadres
Lotte Spekhorst
E-mail: l.s.spekhorst-2@umcutrecht.nl